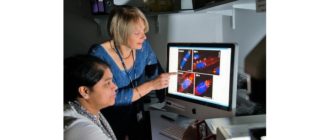
多発性硬化症は、筋肉の衰弱、視力の問題、調整の障害、および身体的麻痺を特徴とする、しばしば衰弱性の自己免疫疾患である。現在、この病気の治療は症状の管理に重点を置いていますが、脳の主要原因に取り組むことができればどうですか?
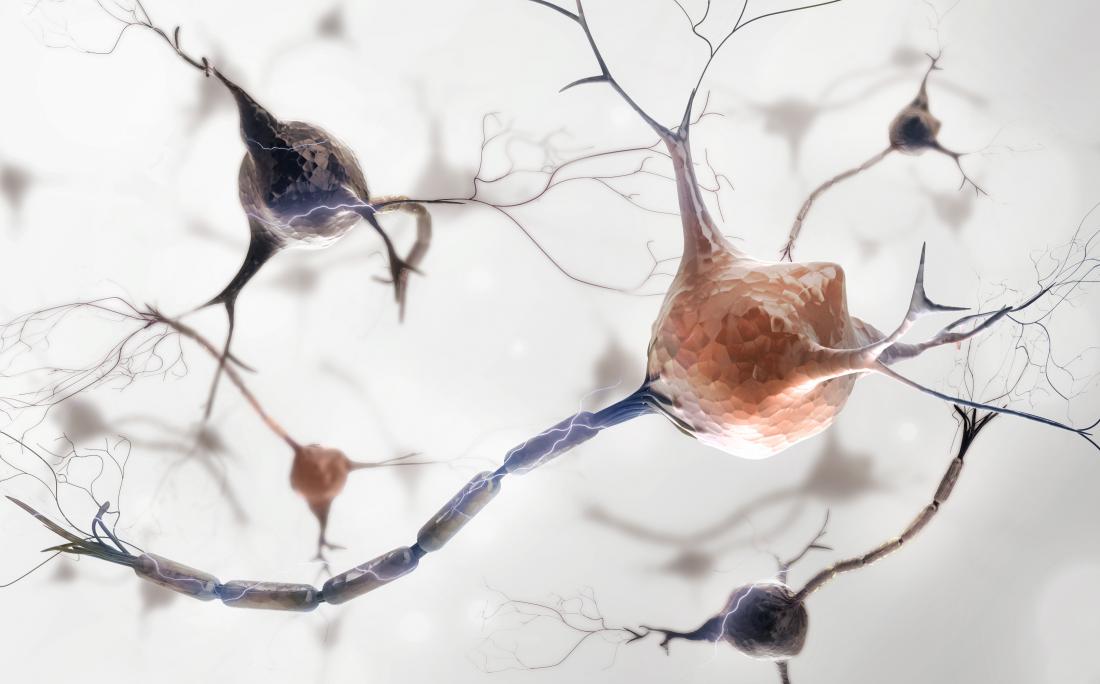
多発性硬化症(MS)の根本原因は不明のままですが、その症状の1つの要因は脱髄であることがわかります。
この過程で、免疫系は、ミエリン、または軸索周囲の「コーティング」を攻撃し、損傷させます。これは、脳と脊髄の神経細胞をつなぐ突起です。
この損傷の結果として、神経細胞の間で伝達される信号が破壊され、したがって、視覚、協調、または筋肉制御の問題が生じる。したがって、MSに特化した研究者の主な課題は、効率的かつ効果的な方法で新しいミエリン「シース」の創出である再ミエリン化を促進する方法でした。
2016年の調査によると、米国の403,600人以上の人々がMSに罹患していますが、以前の研究では、世界中の病気と診断された230万人の推定数が指摘されています。
アクチビン-Aと呼ばれるタンパク質がミエリン修復の促進において重要な役割を果たすことを発見したとき、Veronique Miron博士(英国MS研究のためのエジンバラMS研究センター)および他の科学者は、再ミエリン化研究において画期的な成果をあげました。
当時、彼らはタンパク質がミエリン形成を促進する機構を同定することができなかった。しかし今、ミロン博士とチームは、このタンパク質がどのように修復過程を「スイッチオン」するかを発見しました。
研究者の所見は今や雑誌に掲載されている
‘新しいミエリンを作るように細胞を励ます’
Miron博士らは、アクチビン-Aがインビボ(MSモデルマウスを使用)およびin vitro(MS Society Tissue Bankが提供するヒト組織)の両方に関与するミエリン産生機構を研究した。
研究者らは、ミエリンの産生につながるプロセスは、ミエリンを生成することができるタイプの稀突起神経膠細胞上のアクチビンA受容体2a(Acvr2a)と呼ばれるアクチビン-A受容体の発現に依存することを見出した。
進行性のMSで暮らしていた人々から寄贈された組織サンプルを見ると、Miron博士と彼女のチームは、Acvr2aレベルが再髄鞘形成から恩恵を受けた神経組織において有意に高いことを見出した。対照的に、ミエリン修復の徴候のない組織では、Acvr2aレベルが低下した。
アクチビン-Aは、アクネのミエリン鞘が損傷している部位で乏突起膠細胞に修復作業を開始するように指示するAcvr2aに結合することも発見した。
「このタンパク質アクチビン-Aを最初に発見したとき、ミエロン博士は、再ミエリン化がどのような役割を果たしているのか正確にはわかっていませんでした。 “
再ミエリンジングは疾患の進行を遅らせ、潜在的にそれを停止させるために重要であるため、現在の研究の結果は最終的に新しい薬物標的につながる可能性があるとDr.
「これは、レセプターを標的とする薬物の開発に力を注ぐことができるため、本当にエキサイティングな発見です。MSがこれを行うことができれば、MSが損傷した後に新しいミエリンを作ることができます。
Dr. Veronique Miron
以下に、Miron博士が研究の結果とMSの治療との関連性を説明し、より効果的でより効果的な治療法を指摘するビデオを見ることができます。