骨髄は、股関節および大腿骨を含む身体内の骨のいくつかの内部の海綿質組織である。骨髄には、幹細胞と呼ばれる未成熟細胞が含まれています。
白血病やリンパ腫、鎌状赤血球貧血、その他の生命を脅かす病気のような血液がんを持つ多くの人々は、生存するために骨髄や臍帯血移植に頼っています。
生きるためには健康な骨髄や血球が必要です。疾患が骨髄に影響を与えてもはや効果的に機能しなくなると、骨髄または臍帯血移植が最良の治療選択肢となりうる。一部の患者にとっては、唯一の可能性のある治療法です。
骨髄に関する迅速な事実
骨髄に関する重要なポイントがいくつかあります。詳細は、メインの記事にあります。
- 骨髄は、白血球や血小板とともに、毎日2千億個の赤血球を生産しています。
- 骨髄は、間葉系および造血系の幹細胞を含む。
- 米国では約1万人が骨髄移植を必要とする疾患で毎年診断されています。
- いくつかの病気は骨髄に脅威を与え、骨髄が幹細胞を必須細胞に変えるのを防ぎます。
骨髄とは何ですか?
骨髄は、骨の中心である髄腔を満たす柔らかくゼラチン状の組織である。骨髄の2つのタイプは、骨髄組織として知られる赤色骨髄、および黄色骨髄または脂肪組織である。
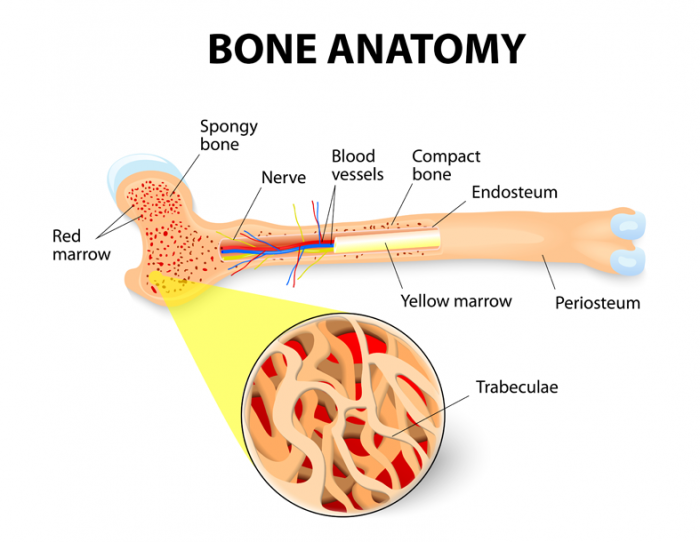
両方のタイプの骨髄には血管や毛細血管が豊富に含まれています2。
骨髄は毎日2千億以上の新しい血液細胞を作り出します8体内のほとんどの血液細胞は骨髄の細胞から発達します5。
骨髄幹細胞
骨髄は、間葉系および造血系の2種類の幹細胞を含む。
赤色骨髄は、造血幹細胞を含有する繊細で血管が強い線維組織からなる。これらは血液を形成する幹細胞です。
黄色骨髄は、骨髄間質細胞としても知られる間葉系幹細胞を含む。これらは脂肪、軟骨、骨を産生する。
幹細胞は、いくつかの異なるタイプの細胞に変わることができる未成熟細胞である。
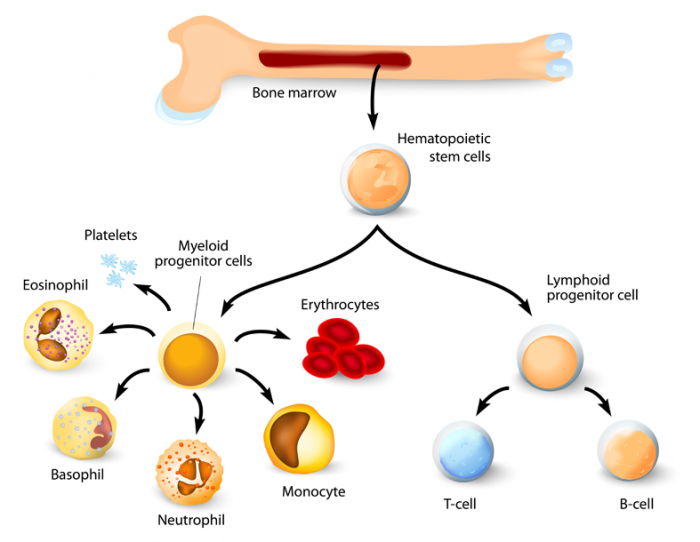
骨髄中の造血幹細胞は、骨髄系およびリンパ系統の2つの主な型の細胞を生じる。これらには、単球、マクロファージ、好中球、好塩基球、好酸球、赤血球、樹状細胞、および巨核球または血小板、ならびにT細胞、B細胞およびナチュラルキラー細胞が含まれる。
異なるタイプの造血幹細胞は、それらの再生能および効力が異なる。
いくつかの細胞は、それらが何種類の細胞を作り出すことができるかによって決定されるように、多分化能、寡占能または単能性である。
多能性造血幹細胞は、以下の特性を有する:
- リニューアル:自分と同じ別のセルを再現できます。
- 分化:より成熟した細胞のサブセットを1つ以上生成することができます。
これらの多能性幹細胞からの異なる血球の発生過程は、造血と呼ばれています。
骨髄移植に必要なのは、これらの幹細胞です。
幹細胞は常に分裂して新しい細胞を産生する。いくつかの新しい細胞は幹細胞として残っており、成熟した血球になる前に前駆細胞や芽細胞として一連の成熟段階を経るものもある。幹細胞は急速に増殖し、毎日数百万の血球を作ります。
血液細胞の寿命は限られています。赤血球の場合、これは100-120日前後です。彼らは絶えず置き換えられています。健康な幹細胞の生産は不可欠です。
未熟な血液細胞が骨髄を離れるのを防ぐために、血管は障壁として働く。
成熟した血液細胞のみが、血管内皮に付着して通過するのに必要な膜タンパク質を含む。しかし、造血幹細胞は骨髄バリアを通過することができる。これらは、末梢血または循環血液から採取することができる。
赤色骨髄の血液を形成する幹細胞は、それぞれ独自の仕事をしている3つの重要なタイプの血液細胞に増殖し、成熟することができます:
- 赤血球(赤血球)は身体の周りで酸素を運ぶ
- 白血球(白血球)は、感染症や病気と戦うのに役立ちます。白血球には、免疫系の根幹であるリンパ球や顆粒球を含む骨髄細胞(好中球、単球、好酸球、好塩基球)が含まれます
- 血小板(血小板)は、損傷後の凝固を助ける。血小板は、別の骨髄細胞である巨核球の細胞質の断片である。
一度成熟すれば、これらの血液細胞は骨髄から血流に移行し、そこでは身体を生き生きと健康に保つために必要な重要な機能を果たします。
間葉系幹細胞は骨髄腔に見出される。それらは、以下のような多数の間質系統に分化する:
- 軟骨細胞(軟骨発生)
- 骨芽細胞(骨形成)
- 破骨細胞
- 脂肪細胞(脂肪組織)
- 筋細胞(筋肉)
- マクロファージ
- 内皮細胞
- 線維芽細胞。
赤い骨髄
赤色骨髄は、ヒト成人では赤血球および血小板を、リンパ球では約60〜70%を産生する。他のリンパ球は赤色の骨髄で生命を始まり、胸腺、脾臓、リンパ節を含むリンパ組織に完全に形成されます1。
肝臓と脾臓と一緒に、赤い骨髄は古い赤血球を取り除く役割も果たします。
黄色骨髄
黄色の骨髄は、主に脂肪の貯蔵庫として働く。それは、生存を提供し、骨が機能するための正しい環境を維持するのに役立ちます。しかし、重度の失血や発熱などの特定の条件下では、黄色の骨髄は赤色の骨髄に戻ることがあります1。
黄色の骨髄は、長い骨の中心空洞に位置する傾向があり、スポンジ状網状骨格内に長い骨梁(梁状構造)を有する赤色骨髄の層によって一般に囲まれている。
骨髄タイムライン
出生前に、骨髄はまず胎盤発達の終わりに向かって鎖骨に発達する。約3週間後にアクティブになります。骨髄は、32〜36週の妊娠期間に主要な造血器官として肝臓から引き継がれます。
新しい連続的な血液形成の必要性が高いため、骨髄は7歳まで赤色のままである。体が老化すると、赤色の骨髄は徐々に黄色の脂肪組織に置き換えられます。成人は平均約2.6kg(5.7lbs)の骨髄を有し、その約半分は赤色である。
成人では、赤色骨髄の最も高い濃度は、脊椎骨、臀部(腸骨)、胸骨(胸骨)、肋骨、頭蓋骨、および腕(上腕骨)および脚の長骨の骨幹端および骨端大腿骨および脛骨)。長骨の他のすべての海綿質、海綿質、骨および中腔は、黄色骨髄で満たされています。
関数
ほとんどの赤血球、血小板、および大部分の白血球は、赤色骨髄で形成されます。黄色の骨髄は、脂肪、軟骨、および骨を産生する。
白血球は数時間から数日、血小板は約10日間、赤血球は約120日間生存する。これらの細胞は、骨髄によって常に置き換えられなければならない。なぜなら、各血液細胞は、予想される寿命を有するからである。
特定の状態は、血液細胞のさらなる産生を誘発し得る。これは、体組織の酸素含有量が低い場合、血液または貧血の喪失がある場合、または赤血球の数が減少した場合に発生する可能性があります。これらが起こると、腎臓は、赤血球を産生するために骨髄を刺激するホルモンであるエリスロポエチンを産生して放出する。
骨髄はまた、感染に応答してより多くの白血球を生成し放出し、出血に応答してより多くの血小板を放出する。人が重度の失血を経験すると、黄色の骨髄を活性化して赤色の骨髄に変換することができます。
健康な骨髄は、さまざまなシステムや活動にとって重要です。
循環系
循環器系は体内のすべての器官やシステムに接触します。これは、様々な機能を備えた多数の異なる細胞を含む。赤血球は酸素を細胞や組織に輸送し、血小板は血液中に運ばれて傷害後血栓を助け、白血球は感染部位や傷害部位に運ばれます。
ヘモグロビン
ヘモグロビンは、赤血球中のタンパク質で、色を与えます。ヘモグロビンは肺の酸素を集め、赤血球に運び、酸素を心臓、筋肉、脳などの組織に放出します。呼吸の廃棄物である二酸化炭素(CO2)もまた、ヘモグロビンによって除去され、肺に送り返されて吐き出される。
鉄
鉄は人間の生理にとって重要な栄養素です。それは赤血球中のヘモグロビンを作るためのタンパク質と結合し、赤血球の生成(赤血球形成)に不可欠です。体は肝臓、脾臓、骨髄に鉄を貯蔵する。ヘモグロビンを作るために毎日必要とされる鉄のほとんどは、古い赤血球の再利用から来ています。
赤血球
赤血球の生成は赤血球生成と呼ばれています。コミットされた幹細胞が完全に機能する赤血球に成熟するには約7日かかります。赤血球が老化するにつれて、活性が低下し、壊れやすくなります。
老化する赤血球は、貪食として知られているプロセスにおいて、一種の白血球またはマクロファージによって除去または摂取される。これらの細胞の内容物は血液中に放出される。この過程で放出された鉄は、新しい赤血球の産生のために骨髄に、または貯蔵のために肝臓または他の組織に運ばれる。
通常、体の総赤血球の約1%が毎日交換されます。健康な人では、毎日約2億億個の赤血球が生産されています。
白血球
骨髄は多くのタイプの白血球を産生する。これらは健康な免疫システムに必要です。彼らは感染を予防して戦う。
白血球または白血球の主なタイプは次のとおりです。
1)リンパ球
リンパ球は骨髄で産生される。彼らは、鼻、口、または他の粘膜を通って体内に入るウイルスによって引き起こされる感染症と戦うための自然抗体を作ります。特定の細胞は、体内に侵入する異種の侵入者(抗原)の存在を認識し、抗原を攻撃するために他の細胞にシグナルを送る。
リンパ球の数は、これらの侵襲に応答して増加する。リンパ球には主に2種類のタイプがあります:Bリンパ球とTリンパ球です。
2)単球
単球は骨髄で産生される。成熟単球は、血液中に平均寿命が3〜8時間しかありませんが、組織に移動するとマクロファージと呼ばれる大きな細胞に成熟します。マクロファージは、細菌、いくつかの真菌、死細胞、および体外の他の物質を包み込んで破壊する、長期間組織内で生き残ることができる。
3)顆粒球
顆粒球は、好中球、好酸球、好塩基球の3種類の白血球に与えられる家族名または集団名です。顆粒球の発生には2週間かかることがありますが、細菌感染などの脅威が増えるとこの時間が短縮されます。
骨髄は、成熟した顆粒球の大部分を貯蔵する。血液中を循環する全ての顆粒球について、骨髄内で血流に放出されるのを待っている細胞が50〜100個存在することがある。結果として、血流中の顆粒球の半分は、感染を検出してから7時間以内に身体内の感染と積極的に戦うことができる。
顆粒球が一旦血液を離れると、通常は戻ってこない。顆粒球は、条件に応じて4〜5日間まで組織内で生存することができるが、循環中では数時間しか生存しない。
4)好中球
好中球は最も一般的な顆粒球である。彼らは細菌やウイルスを攻撃して破壊することができます。
5)好酸球
好酸球は、多くのタイプの寄生虫感染および寄生虫および他の生物の幼虫に対する闘いに関与している。彼らはまた、いくつかのアレルギー反応にも関与しています。
6)好塩基球
好塩基球は、白血球の最も一般的でないものであり、ヒスタミン、ヘパリンおよび他の物質の放出を引き起こす様々なアレルゲンに応答する。
ヘパリンは抗凝固剤です。血液が凝固するのを防ぎます。ヒスタミンは、炎症および炎症を引き起こす血管拡張剤である。これらの物質を放出することにより、病原体がより透過性になり、白血球およびタンパク質が組織に侵入して病原体に関与することが可能になる。
アレルゲンの影響を受ける組織の炎症および炎症は、枯草熱、いくつかの喘息、蕁麻疹、および最も重篤な形態のアナフィラキシーショックで見られる反応の一部である。
血小板
骨髄は、血栓形成として知られる過程で血小板を産生する。血液が凝固し、血餅が形成され、出血を止めるためには血小板が必要である。
突然の失血は、傷害または創傷の部位での血小板活性を引き起こす。ここで、血小板は互いに凝集し、他の物質と結合してフィブリンを形成する。フィブリンは糸状構造を有し、外部の痂皮または凝塊を形成する。
血小板の欠乏により、体が挫傷しやすくなり、出血がより容易になる。血が開いた傷口でうまく凝固しないことがあり、血小板数が非常に低い場合、内出血のリスクがより高くなる可能性があります。
リンパ系
リンパ系は、骨髄、扁桃腺、胸腺、脾臓およびリンパ節などのリンパ管器官からなる。
全てのリンパ球は、幹細胞と呼ばれる未成熟細胞から骨髄に発生する。胸腺で成熟したリンパ球(胸骨の後ろ)はT細胞と呼ばれます。骨髄やリンパ器官で成熟したものはB細胞と呼ばれています。
免疫系
免疫系は、身体を病気から守ります。体に侵入する可能性のある細菌やウイルスなどの望ましくない微生物を殺します。
免疫系は感染とどのように戦うのですか?
リンパ節と呼ばれる小さな腺が体全体に散在しています。リンパ球が骨髄で作られると、リンパ節に移動します。次いで、リンパ球は、血管に空になった大きな排液管で出会うリンパチャネルを介して各節間を移動することができる。リンパ球はこれらのダクトを通って血液に入る。
リンパ球の3つの主要なタイプが免疫系の重要な役割を果たす:
Bリンパ球(B細胞)
これらの細胞は、哺乳動物の骨髄の造血幹細胞に由来する。
B細胞は、細胞の表面上にB細胞受容体(BCR)を発現する。これらは、侵入する微生物または他の抗原性物質の表面上の抗原に細胞を付着させる。
この理由から、B細胞は、免疫系の他の細胞に侵入する微生物を警告するので、抗原提示細胞として知られている。
B細胞はまた、感染を引き起こす微生物の表面に付着する抗体を分泌する。これらの抗体はY字型であり、それぞれが一致する抗原「キー」が適合する特殊な「ロック」に類似している。このように、各Y型抗体は異なる微生物と反応し、感染との戦いを目的としてより大きな免疫系反応を誘発する。
状況によっては、B細胞は、人体の正常細胞を、免疫系応答を必要とする抗原であると誤って識別する。これは、多発性硬化症、強皮症、および1型糖尿病などの自己免疫疾患の発症の背後にある機構である。
Tリンパ球(T細胞)
これらの細胞は、胸腺(胸腺の成熟したいくつかのT細胞)のすぐ後ろにある胸腺の小さな臓器である胸腺に成熟しているため、いわゆるです。多くの異なるタイプのT細胞が存在し、それらは適応細胞性免疫の一部として様々な機能を果たす。 T細胞は、B細胞が侵入する細菌、ウイルスまたは他の微生物に対する抗体を作製するのを助ける。
B細胞とは異なり、いくつかのT細胞は、微生物の表面上の抗原に結合した後、直接に病原体を包み込み破壊する。
先天性免疫系のナチュラルキラー細胞と混同されないナチュラルキラーT細胞は、適応性のある自然免疫系を架橋する。 NKT細胞は、他の多くの抗原とは異なる方法で提示された抗原を認識し、Tヘルパー細胞および細胞傷害性T細胞の機能を果たすことができる。彼らはまた、いくつかの腫瘍細胞を認識し除去することができる。
ナチュラルキラー(NK)細胞
これらは、ウイルスに感染した細胞を直接攻撃するリンパ球の一種です。
移植
骨髄移植は、様々な理由で使用することができます。
- 罹患した機能不全の骨髄を、健康に機能する骨髄と置き換えることができる。これは、白血病、再生不良性貧血、および鎌状赤血球貧血などの病気に使用されます。
- 化学療法や放射線療法で死亡していない既存のまたは残存する白血病や他のガンと戦う新たな免疫システムを再生成することができます。
- 高用量の化学療法または放射線が悪性腫瘍を治療するために与えられた後、骨髄を置換し、その正常な機能を回復することができる。
- ハーラー症候群や副腎白質ジストロフィーなどの遺伝病のプロセスによるさらなる損傷を防ぐために、骨髄を遺伝的に健康で機能する骨髄に置き換えることができます。
幹細胞は主に4つの場所にあります:
- 胚
- 骨髄
- 末梢血、身体全体の血管に見られる
- 臍帯血は、臍帯で発見され、出生後に収集9
移植のための幹細胞は、胎児を除いてこれらのいずれかから得られる。
造血幹細胞移植は、骨髄、末梢血、または臍帯血から採取した幹細胞の静脈内注入を含む。
これは、骨髄や免疫系が損傷しているか欠陥のある患者の造血機能を再確立するために使用されます。
血液・骨髄移植のための世界的ネットワークの第1回報告書によると、50,000以上の最初の造血幹細胞移植手順、28,000の自己移植手順、21,000の同種異型移植手順が毎年世界中で行われています。
この数字は毎年10〜20%増加し続けています。臓器損傷、感染、および重度の急性移植片対宿主病(GVHD)の減少は、改善された転帰に寄与しているようである。
血液悪性腫瘍の自己造血幹細胞移植(HSCT)後少なくとも2年生存した854人の患者の研究では、移植後10年で68.8%が生存している
骨髄移植は、白血病などの骨髄機能を脅かす病気のための主要な治療法です。
移植は、血液細胞を生産してその数を正常なレベルにするための身体の能力を再構築するのに役立ちます。骨髄移植で治療することができる病気には、癌性疾患および非癌性疾患の両方が含まれる。
癌性疾患は、血液細胞に特異的に関与していてもいなくてもよいが、癌治療は、新しい血液細胞を製造する身体の能力を破壊する可能性がある。
がん患者は、通常、移植前に化学療法を受けます。これは、損なわれた骨髄を排除します。
マッチするドナーは、ほとんどの場合、近親者であり、移植のために収穫され準備された骨髄を有する
骨髄移植のタイプ
骨髄移植のタイプには、
- 自己移植:患者は、末梢または臍帯血から採取した幹細胞を骨髄に補充する
- 同系移植:患者は、同一の双子から幹細胞を受け取ります
- 同種異系移植:患者は、兄弟、親または無関係のドナーから一致する幹細胞を受ける
- 孤立性移植:HLA同一マッチングドナーを持たない患者の約70%の治療選択肢
- 臍帯血:同種異系移植の一種。誕生直後に新生児の臍帯から幹細胞を除去する。幹細胞は移植のために必要となるまで凍結保存されます。臍帯血細胞は非常に未成熟であるため、マッチングの必要性は少なくなりますが、血球数の回復にはかなり時間がかかります。
組織タイプ
人の組織タイプは、体の大部分の細胞の表面上のヒト白血球抗原(HLA)のタイプとして定義される。 HLAは、細胞が身体に属しているか否かを決定するのを助けるために身体が使用するタンパク質またはマーカーである。
組織の種類が適合しているかどうかを確認するために、医師はドナーとレシピエントの血液細胞の表面に一致するタンパク質の数を評価します。何百万もの組織タイプがありますが、いくつかは他のタイプよりも一般的です。
組織タイプは継承され、タイプは各親から継承されます。これは、親族がマッチする組織タイプを持つ可能性が高いことを意味します。
しかし、家族から適切な骨髄ドナーが見つからない場合、医師は骨髄ドナー登録簿に適合する組織タイプの人を見つけようとします。
移植前のテスト
潜在的な問題を特定するために、骨髄移植の前にいくつかの検査が行われる。
テストには以下が含まれます:
- 組織タイピングおよび様々な血液検査
- 胸部X線
- 肺機能検査
- CTまたはCATスキャン
- 心電図および心エコー(ECG)を含む心機能検査、
- 骨髄生検
- 骨格調査
さらに、骨髄移植の前に完全な歯科検診が必要であり、感染リスクを軽減することができます。患者の感染リスクを軽減するために移植前に他の予防措置を講じることもあります。
骨髄を収穫する
骨髄生検および骨髄吸引による検査のために骨髄を得ることができる。
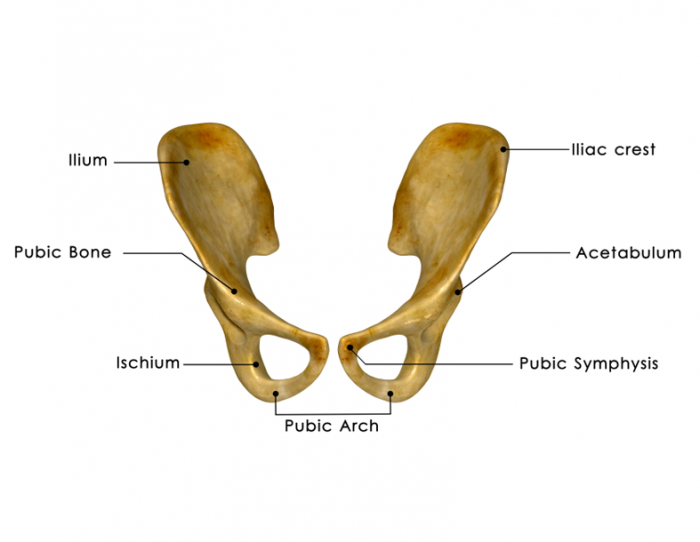
骨髄収穫は比較的日常的な手順となっている。ドナーが全身麻酔下にある間に後腸骨稜から吸引される17。
それはまだかなりの量の赤色骨髄を含んでいるので、胸骨から、および子供の上脛骨から採取することもできる。
医師は、通常は股関節の骨に針を挿入し、骨髄の一部を引き抜く。それは保存され、凍結されます。
国家骨髄ドナープログラム(NMDP)によって確立されたガイドラインは、除去された骨髄の量をドナーの体重の15mL / kgに制限する。自己および同種骨髄移植片に移植を確立するためには、1キログラム当たり1×103および2×108個の骨髄単核球の用量が必要である。
骨髄収穫に関連する合併症はまれです。麻酔、感染、出血に関連する問題があります。
骨髄機能を評価する別の方法は、骨髄から循環血液への幹細胞の放出を刺激する特定の薬物を与えることである。その後、血液サンプルを採取し、顕微鏡検査のために幹細胞を単離する。新生児では、幹細胞を臍帯から回収することができる。
骨髄はどのように移植されていますか?
移植の前に、化学療法、放射線、またはその両方を与えることができる。これは2つの方法で行うことができます。
- 切除(骨髄破壊的)治療:癌細胞を死滅させるために、高用量の化学療法、放射線、またはその両方を投与する。これはまた、残っている健康な骨髄をすべて死滅させ、新しい幹細胞を骨髄内で増殖させる
- 低強度治療、またはミニ移植:患者は移植前に低用量の化学療法および放射線を受ける。これにより、高齢の患者および他の健康問題を有する患者に移植が可能になる。
幹細胞移植は、通常、化学療法および放射線が完了した後に行われる。
骨髄または末梢血の注入は、ベッドサイドで行われる比較的簡単なプロセスである。骨髄生成物を数時間にわたってIV管を介して中心静脈を通して注入する。自己由来の製品はほとんど常に凍結保存されています。彼らはベッドサイドで解凍され、数分の間に急速に注入される。
血流に入った後、造血幹細胞は骨髄に移動する。そこでは、生着として知られているプロセスで、新しい白血球、赤血球、および血小板を生産し始めます。移植は通常、移植後2〜4週間に起こる。
ほとんどの場合、最小限の毒性が認められています。 ABOミスマッチの骨髄注入は時には溶血反応につながることがあります。幹細胞の凍結保存に使用されるジメチルスルホキシド(DMSO)は、顔面紅潮、喉のくすんだ感覚、口の強い味(ニンニクの味)を引き起こす可能性があります。まれに、DMSOは徐脈、腹痛、脳症または発作、および腎不全を引き起こすことがある。
DMSO 2g / kg /日を超える用量で起こる脳症の危険性を避けるために、500mLを超える幹細胞輸液を2日間にわたって注入し、輸液速度を20mL /分に制限する。
医師は定期的に血球数をチェックします。免疫機能の完全な回復は、自家移植レシピエントの場合は数ヶ月、同種移植または同系移植を受けた患者の場合は1〜2年かかる場合があります。
血液検査は、新しい血液細胞が産生されていることを確認し、がんが戻っていないことを確認します。骨髄吸引はまた、医師が新しい骨髄がどれくらいうまく機能しているかを判断するのに役立ちます。
リスク
HSCTに関連する合併症には、早期効果および後期効果の両方が含まれる。
早期に発生する問題には、
- 粘膜炎
- 出血性膀胱炎
- 長期の重度の汎血球減少症
- 感染
- GVHD(移植片対宿主病)
- 移植不全
- 肺合併症
- 肝臓静脈閉塞性疾患
- 血栓性細小血管症
遅れて発生する問題には、
- 慢性GVHD
- 眼の効果
- 内分泌作用
- 肺作用
- 筋骨格系の効果
- 神経学的効果
- 免疫効果
- 感染
- うっ血性心不全
- その後の悪性腫瘍
主なリスクには、感染症、貧血、移植不全、呼吸窮迫、および過剰な体液への感受性の増加が含まれ、肺炎および肝臓機能不全に至り得る。
ドナー組織とレシピエント組織との間のミスマッチは、宿主細胞と移植片の細胞との間の免疫反応を引き起こす可能性がある。
移植細胞が宿主細胞を攻撃する場合、結果は移植片対宿主病(GVHD)と呼ばれる危険な状態であり、急性または慢性であり、皮膚発疹、胃腸疾患または肝臓疾患として現れることがある。 GVHDの危険性は、慎重な組織適合によって最小限に抑えることができる。
ドナー抗原の一致が同じであっても、レシピエントの約40%がGVHDを発症し、1つの抗原のみがミスマッチの場合は60〜80%に上昇する。この合併症の危険性のために、自己移植がより一般的に行われている。
50歳以上の患者には、30年以上の死亡率や罹患率が高く、GVHDの発生率が高いため、骨髄移植はこれまで推奨されていませんでした。しかし、多くの移植センターでは、50歳をはるかに超える患者で骨髄移植を成功させています。
削除されたものに取って代わる新しい骨髄を生み出すため、寄付者にはほとんどリスクはありません。しかし、感染のわずかなリスクがあり、麻酔に対する反応は任意の外科的処置で起こり得る。
病気
骨髄が多くの身体系に影響を及ぼすため、問題は血液に影響を及ぼす癌を含む広範な疾患を引き起こす可能性があります。
多くの病気は、骨髄が幹細胞を必須細胞に変えるのを防ぐため、骨髄に脅威を与えます。
白血病、ホジキン病および他のリンパ腫が、骨髄の生産能力を損ない、幹細胞を破壊することが知られている。
骨髄検査は診断に役立ちます:1
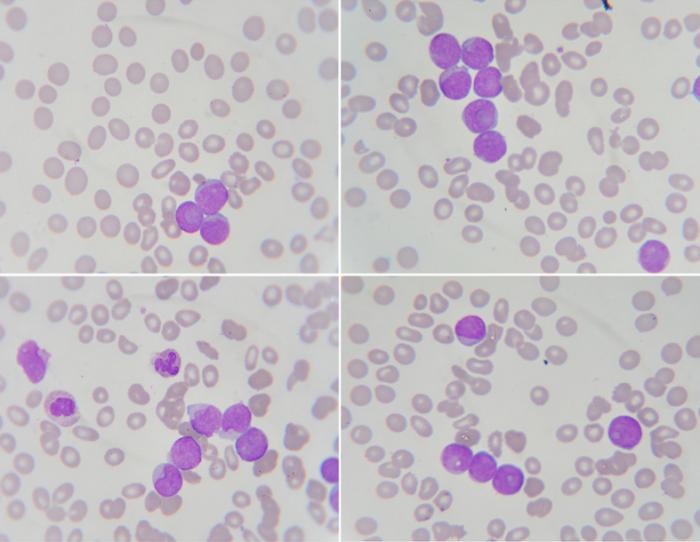
- 白血病
- 多発性骨髄腫
- ゴーシェ病
- 異常な貧血症
- 他の血液疾患。
造血幹細胞移植(HSCT)で治療できる疾患の数が増えています。
多発性骨髄腫および非ホジキンリンパ腫を治療するために、自家移植の半分以上が行われる。大部分の同種異系移植は、血液学的およびリンパ性癌のために行われる。
米国では4分ごとに、誰かが血液がんの診断を受けます。骨髄移植はしばしば生存のための最良の機会です。
患者のおよそ30%が家族内でマッチするドナーを見つけることができますが、毎年70%、または約14,000人が無関係の人から寄付された骨髄に頼っています。
自己HSCTは現在以下の治療に使用されています:
- 多発性骨髄腫
- 非ホジキンリンパ腫
- ホジキンリンパ腫
- 急性骨髄性白血病
- 神経芽細胞腫
- 胚細胞腫瘍
- 自己免疫障害、例えば全身性エリテマトーデスおよび全身性硬化症
- アミロイドーシス
同種異系HSCTは、以下を治療するために使用される:
- 急性骨髄性白血病
- 急性リンパ芽球性白血病
- 慢性骨髄性白血病
- 慢性リンパ球性白血病
- 骨髄増殖性疾患
- 骨髄異形成症候群
- 多発性骨髄腫
- 非ホジキンリンパ腫
- ホジキンリンパ腫
- 再生不良性貧血
- 純粋な赤血球形成不全
- 発作性夜間ヘモグロビン尿症
- ファンコニ貧血
- サラセミアメジャー
- 鎌状赤血球貧血
- 重症複合免疫不全(SCID)
- ウィスコット・アルドリッチ症候群
- 血液貪食リンパ組織球増数症
- ムコ多糖症などの代謝に関連する遺伝的障害
- ゴーシェ病、異染性白質ジストロフィー、および副腎白質ジストロフィー
- 表皮水疱症
- 重度の先天性好中球減少症
- シュワックマン – ダイアモンド症候群
- ダイヤモンド・ブラックファン貧血
- 白血球接着欠損症
HSCTは次の治療にも役立ちます。
- これは確認されていませんが、乳がん
- 精巣癌、一部の患者では初期段階
- いくつかの遺伝学的免疫または造血障害
癌を治療するために使用される高用量化学療法および放射線療法などの特定の治療の後に、骨髄移植が必要とされることがあります。これらの治療は健康な幹細胞を破壊し、癌細胞を破壊する傾向があります。
骨髄検査
骨髄検査は、特定の疾患、特に血液および血液形成器官に関連する疾患の診断に役立ちます。検査は鉄の貯蔵と血液生産に関する情報を提供します.1
骨髄吸引は、中空針を用いて、顕微鏡下での検査のために骨髄の小さな試料(約1ml)を除去する。
針は、通常、成人の股関節または胸骨および小児の脛骨の上部(下腿のより大きい骨)に挿入され、吸引は試料を抽出するために使用される。
骨髄吸引は、典型的には、以前の血液検査によって示される場合に行われ、未熟な血液細胞の様々な段階に関する情報を提供するのに特に有用である。
寄付
骨髄寄贈には2つの主要な種類があります。
最初の方法は、骨盤の骨から骨髄を取り除くことです。
第2のより一般的な方法は、末梢血幹細胞(PBSC)寄贈と呼ばれています。これは、血液から幹細胞を直接ろ過することを含む。これらの血液幹細胞は、骨髄そのものではなく、血液癌やその他の病気の治療に必要です。
個体が骨髄寄贈レジストリに加わると、患者の医師が適切と考える方法を用いて寄付することに同意している。
費用の面では、骨髄寄贈の費用は、通常、NMDPまたは患者の医療保険のいずれかによってカバーされます。ドナーは決して寄付金を支払うことはなく、寄付することは決してありません。
ドナーへのリスクは最小限です。ドナーの99%以上が手術後に完全回復する。血行献血の場合、主なリスクは処置自体の間に麻酔を使用することです。
PBSCの寄付では、血液を機械でろ過する手順自体は危険とはみなされません。
適切な骨髄ドナーを見つける機会は、民族性に応じて66〜93%です。
骨髄8を寄付することができる人
以下は、骨髄ドナープログラム(NMDP)が推奨する骨髄寄贈に関する一般的なガイドラインです。
このガイドラインは、ドナーとレシピエントの健康と安全を守ることを目的としています。寄付者は、特定の詳細については地元のNMDPセンターに連絡し、医療チームとの献金について話し合うことが奨励されます。
- 登録簿に記載されるためには、潜在的なドナーは健康で、18歳から60歳の間でなければなりません。
- 移植を必要とする人と合っている場合、各ドナーは健康診断を受け、感染のない状態で寄付する必要があります。
- 薬を使用した人々は、健康であり、彼らが持っている病状が寄付の時点で管理されている限り、通常、骨髄を寄付することができます。
許容される薬物には、避妊薬、甲状腺薬が含まれる。抗ヒスタミン剤、抗生物質、処方点眼剤、および皮膚クリームのような局所的薬剤が挙げられる。抗不安薬や抗うつ薬は、その状態が制御されている限り許されます。
寄付はできません:
- 妊娠中の
- 医師によって処方されていない静脈内薬を使用する者
- その人がB型肝炎またはC型肝炎の陽性血液検査を受けた場合
- ほとんどのタイプの癌または特定の心臓病などの特定の病状を有する患者
ライム病、マラリア、または最近の入れ墨やピアスを患っている人は、骨髄を寄付する前に少なくとも1年間は待つべきです。
骨髄の一致はどのように決定されますか?
寄付に登録した後、患者は潜在的なドナーと患者を突き合わせるために使用されるHLAタイピング試験に着手する。
彼らのHLAタイプは、潜在的なドナーのデータベースに追加され、医師はレジストリを検索して、患者のためのマッチを見つけようとします。
血液細胞中のタンパク質は、それらがレシピエントのタンパク質と類似しているかどうかを比較するために比較される。一致した場合、潜在的なドナーに連絡が取られます。
ドナーの組織タイプが患者の組織タイプに類似しているほど、患者の身体が移植を受け入れる機会が増えます。
骨髄ドナーズ・ワールドワイド(BMDW)は、43カ国の59の登録簿と21カ国の37の臍帯血登録簿の集合データベースである。 2615万人の潜在的な幹細胞ドナーと687千の臍帯血ユニットが2015年9月現在利用可能であった19.19,20。NMDPによる予備調査でもBMDWを定期的に探索している。
骨髄を寄付するとどうなりますか?
造血幹細胞ドナーについて以下の研究が日常的に行われている:

- 歴史と身体検査
- 血清クレアチニン、電解質、肝機能研究
- (CMV)、ヘルペスウイルス、HIV RNA、抗HIV抗体、B型肝炎ウイルスおよびC型ウイルス、ヒトT細胞リンパ球向性ウイルス-1/2(HTLV-I / II)および梅毒(VDRL)の血清学的研究;自己献血では、CMVおよびVDRL検査は不要です
- ABO血液型判定
- HLAタイピング
- 胸部X線撮影
- 心電図(ECG)
末梢血幹細胞(PBSC)を寄付することは、
PBSCに寄付する前に、手順に沿って5日間、フィルグラスチムと呼ばれる薬を毎日注射する必要があります。この薬は骨髄から幹細胞を採取するので、供血者はその中でより多くを循環させるでしょう。
PBSCに寄贈するには、アフェレーシスとして知られている手順が必要です。これは、一方の腕に挿入され、機械を通過したカテーテルを用いて体から血液を採取し、血小板および白血球とともに幹細胞をろ過するときである。残りの血液(主に血漿および赤血球からなる)は、他方の腕の静脈を通って体内に戻る。
この手順は完全に無痛であり、血漿を提供することと同様である。 PBSCの寄付には通常2〜4時間が必要で、2〜6時間持続します。
PBSCの寄付は麻酔を必要としません。骨髄から血流への幹細胞の動員(放出)を刺激するために与えられる投薬は、骨や筋肉の痛み、頭痛、疲労、悪心、嘔吐、または睡眠障害を引き起こす可能性がある。これらの副作用は、通常、投薬の最後の投与から2〜3日以内に停止する。
骨髄を寄付する
PBSCの代わりに実際の骨髄を寄付している人は、フィルグラスチム注射の必要はありません。骨髄献血は、手術室で行われる外科的処置であり、麻酔が必要であり、したがって完全に無痛である。手順全体には1〜2時間かかります。
96%の症例では、全身麻酔薬が使用されます。これは、ドナーが全手順で無意識になることを意味します。少数の場合、局所麻酔薬が使用され、骨髄が採取される領域を単純に麻痺させる。この状況では、その人は手術中に目を覚ますでしょう。
人は胃の上に横たわっている。医師は、骨盤の両側に約4分の1インチの長さの切開を行う。その後、特別な中空の針を骨に挿入し、骨髄を介して骨髄を採取する。切開部は、通常、ステッチを必要としない。
手術後、ドナーは意識を回復するまで回復室にいます。彼らが食べ、飲んで歩くことができれば、彼らは去ることができます。
回復
寄付後、特に手術が必要な場合は、完全な回復に数日かかることがあります。
骨髄を寄付している人は、しばしば頭痛、疲労、筋肉痛、背中や腰の痛み、切開部位周辺の挫傷、および歩行困難を経験する。これは、最大2日間、または数週間続くことがあります。
PBSCに寄付をした人は、針の傷跡以外の寄付に続く副作用を経験することはまずありません。回復時間はほぼ即時です。
寄付後、骨髄は4〜6週間で元の状態に戻ります。
結果
骨髄移植の成果は、
- 移植のタイプ
- どのくらいのセルが一致するか
- 患者がどのようなタイプの状態にあるか
- 患者の年齢および全体的な健康状態
- 移植前に使用される化学療法または放射線療法の種類および投与量
- 合併症
病状が安定している患者または寛解している患者は、後期に移植を受けた患者または再発した病気に罹患した患者と比較して、良好な転帰のより良い機会を有する。移植時の若年者も、機会を改善する。
非悪性疾患のための移植は、ドナーが兄弟である場合に70〜90%、ドナーが無関係である場合に36〜65%の生存率で、より好ましい結果を生じる傾向がある。
移植時の寛解時の急性白血病の移植は、ドナーが関連する場合は55〜68%、ドナーが無関係なら26〜50%の生存率を有する。
骨髄移植は、完全にまたは部分的に病気を治癒することがある。移植が成功すれば、十分に気分が良いとすぐに、ほとんどの正常な活動に戻ることができます。通常、フルリカバリには最大1年かかります。