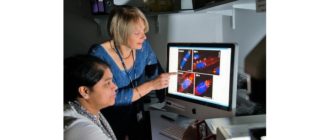
新しい研究は、この生命を脅かす脳腫瘍の成長を止める方法を特定した後、グリア芽細胞腫患者のための新しい治療法の新鮮な希望をもたらします。
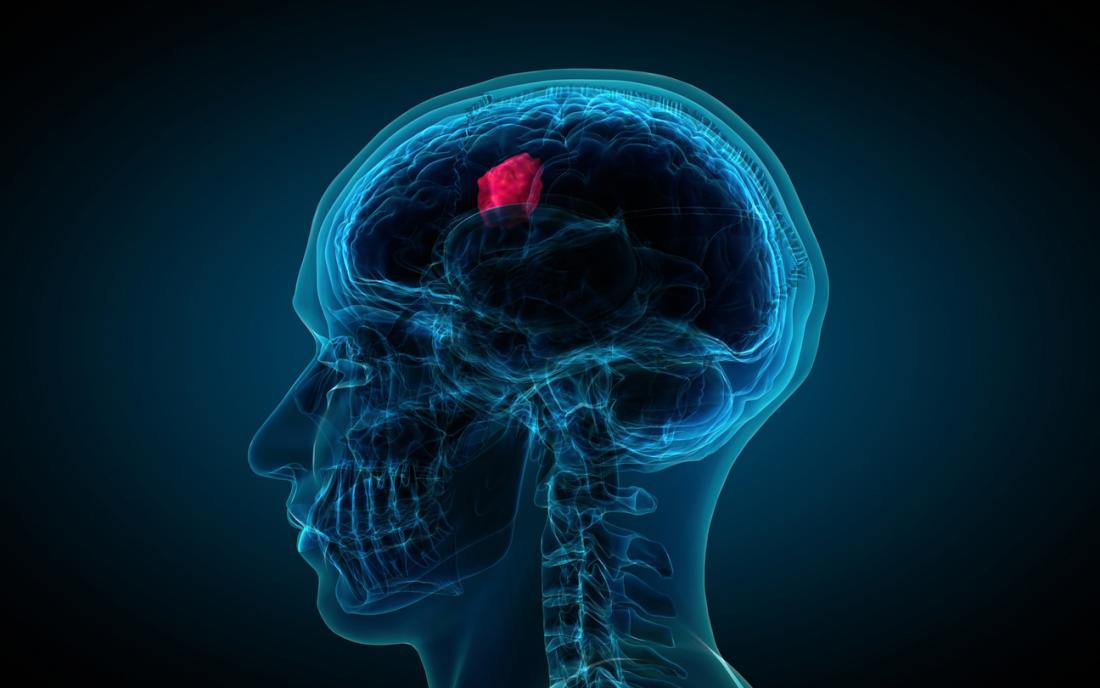
ボストンのマサチューセッツ工科大学(MIT)の科学者は、PRMT5と呼ばれる特異的なタンパク質がグリア芽細胞腫の増殖を促進するメカニズムを明らかにしました。
さらに、既存の薬物のクラスを用いてこのメカニズムを阻止することにより、マウスにおいてグリア芽細胞腫の腫瘍増殖を阻止することができた。
研究の当時、MITのポスドクの学生であった研究代表者のChristian Braun氏と同僚は最近、研究結果を雑誌に掲載しました。
グリア芽細胞腫(多形性グリア芽細胞腫とも呼ばれる)は、星状細胞と呼ばれる星状グリア細胞から形成される悪性脳腫瘍の一種です。
American Brain Tumor Associationによると、今年米国では約80,000例の原発性脳腫瘍が新たに診断されると予想されています。これらのうち、膠芽腫は約14.9%を占める。
グリア芽細胞腫は最も一般的な脳腫瘍ではありませんが、最も致死的です。患者の化学療法および放射線療法を受けた場合、グリア芽腫の診断後わずか14.6ヶ月である。
このように、神経膠芽細胞腫を予防および治療するための新しい治療法を特定することが切望されている。ブラウンらは、研究成果がこの目標を達成するのに役立つと信じています。
PRMT5および遺伝子スプライシング
以前の研究では、MITの生物学科のBraun氏と彼の同僚であるMonica Stanciuは、PRMT5が神経膠芽細胞腫の可能性のあるドライバであることを明らかにしましたが、タンパク質がそうする正確なメカニズムは不明でした。
この知見は、PRMT5が神経膠芽腫の増殖を促進する独特の形態の「遺伝子スプライシング」に関与している可能性があることを示した。
研究者らは、遺伝子スプライシングは、イントロンと呼ばれるメッセンジャーRNA(mRNA)の部分がmRNA鎖に「切断」されるプロセスであると説明しています。
その後の研究では、約1〜3個の「拘留されたイントロン」がヒトmRNA鎖の約10〜15%に存続し、これらの残りのイントロンはmRNA分子が細胞核を離れることを妨げることが明らかになった。
「これらの鎖は基本的にmRNAリザーバであると考えています」と、ミュンヘンのルードヴィヒ・マクシミリアン大学を拠点にしているブラウンは述べています。 「これらの非生産的なアイソフォームを核に置いておけば、それらが翻訳されないようにする唯一の方法はそのイントロンです」
彼らの最新の研究では、仮説の通り、研究者らは、PRMT5が独自の遺伝子スプライシングプロセスにおいて重要な役割を果たすことを見出した。彼らは、脳幹細胞が高レベルのPRMT5を有することを示唆しており、これは細胞の増殖、成長および分裂に関連する遺伝子の効果的なスプライシングおよびより大きな発現を確実にするために使用される。
「細胞が成熟状態に近づくにつれて、PRMT5レベルが低下し、イントロンレベルが上昇し、増殖に関連したメッセンジャーRNAが核に突き当たる」とThe David H. Koch Institute of Integrativeの共同研究者、Jacqueline Leesは説明する。 MITにおけるがん研究。
彼らは、癌性脳細胞では、PRMT5のレベルが再び増加し、これが独特の遺伝子スプライシングプロセスを活性化し、癌細胞が制御不能に成長することを促進することを説明している。
マウスにおける膠芽腫の成長停止
研究者らは、ヒト膠芽細胞腫細胞におけるそれらの発見をさらに確認した。 PRMT5がPRMT5タンパク質の産生を阻害することを阻害すると、細胞増殖と分裂が停止することが分かった。
研究者はまた、PRMT5阻害剤でマウスモデルを治療することによって、膠芽細胞腫腫瘍の成長を停止させることができた。
この研究に関与していないニューヨークのメモリアルスローンケタリングがんセンターのオマル・アブデル・ワハブ氏は、「この研究には多くの役割があり、今までは何が癌への貢献にとって本当に重要な経路です」
「RNAのスプライシング機構が重要な役割を果たしており、さらにRNAスプライシングが破壊されると、その重要な経路は無効になる」と彼は付け加えた。
さらに、この研究では、PRMT5阻害剤での治療にうまく反応する可能性のある患者を特定するために使用できるバイオマーカーが同定されました。
この研究は、グリア芽細胞腫の根底にある原因を明らかにするだけでなく、この致命的な癌に対する新しい予防および治療戦略の扉を開くかもしれない。