治癒困難な筋肉消耗性疾患(エメリードレフュス筋ジストロフィー)の原因が初めて明らかにされた、と科学者は主張している。
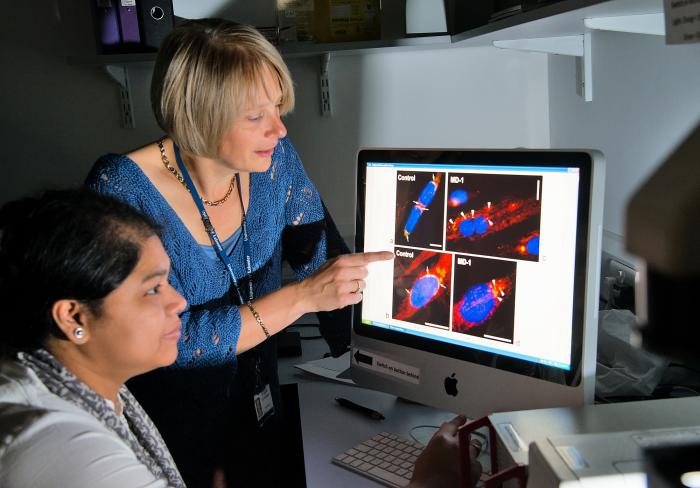
Emery-Dreifuss筋ジストロフィー(EDMD)は、筋肉の消耗および関節の硬化を引き起こす遺伝性の状態である。この症状は小児期に始まり、患者が後の人生で移動性を著しく低下させるという点で悪化する。
EDMD患者が成人に達する時までに、心臓発作の危険性が高い心臓病を発症し、ペースメーカを挿入する必要があります。
この新しい研究の背後にある研究者は、一部の患者では、EDMDが、各細胞の核のための「足場」を産生する遺伝子の変異によって引き起こされると述べている。
しかしながら、すべてのEDMD患者の約半数において、同定された遺伝子のいずれにおいても突然変異は同定されていない。
現在、英国のレスター大学生化学シニア講師Sue Shackleton博士の後ろのリード研究者は、これらの患者の一部でEDMDを引き起こす原因となる2つの新しい遺伝子(SUN1とSUN2)をどのように同定したかを説明しています。
新しく同定された突然変異はどのようにEDMDに寄与するか?
以前に核足場の完全性を損なうと同定された遺伝子突然変異と同様に、SUN1およびSUN2も足場構造の一部を形成するタンパク質を産生する。
突然変異したバージョンのSUN1およびSUN2は、核と細胞の残りの間の接続を妨害し、結果として核が筋細胞内に異常に位置付けられる。
Shackletonは、「核は筋肉細胞の縁に固定されている」と説明している。「おそらく、筋収縮に関与する細胞の主要な構造の仕方には入らない」
彼女は、この誤った配置が核に損傷を与え、筋収縮を損なう可能性があり、筋肉の疲労と衰弱につながると付け加えている。
「筋肉核の位置が正しくないと、EDMDの症状を引き起こす原因になると我々は考えている」
この発見は、「今後この疾患の治療のための新規な薬剤標的の可能性を提供する」と彼女は言う。
しかし、Shackletonは、病気のメカニズムを調べ、健康な筋肉細胞内の核の位置の理解を高めるためにはさらなる研究が必要であると述べている。
リンクされたコメントでは、筋ジストロフィー運動の研究責任者、Marita Pohlschmidt博士は、この研究の結果を歓迎します。
Pohlschmidt博士は、「将来的には、より多くの人々に正確な遺伝子診断を提供するだろう」と語る。「家族に計画を立てる際の情報提供の選択肢を子供に伝えるリスクを理解する助けになる」
「正確な遺伝子診断は、患者が病状の予後に関するより正確な情報を得ることを意味する」と付け加えている。最も重要なことは、この複雑で壊滅的な状態の治療法の開発においては、 “
今年3月、Weill Cornell医学大学院のニューヨークに拠点を置く科学者とSloan Kettering Memorial Sloan-Kettering Cancer CenterのSloan Kettering Instituteが、偏在していない骨格筋細胞がEDMDにどのように関係しているかを調べました。
フルマシンの胚および幼虫の筋肉において、科学者は日曜日のドライバー(またはSyd)遺伝子に突然変異を起こし、EDMDの特徴である不均一に間隔をあけてクラスター化された核を生じた。これらの異常に位置する核との関係は弱いクローラー人間の病気の状態を模倣しています。